視床下部の未知の神経細胞が発見され、新たな肥満治療の可能性が浮上
肥満は、米国の成人の40%、子供の20%に影響を与える深刻な健康問題です。最近では、新しい治療法が注目を集め、肥満の管理に一定の成果を上げていますが、脳と体の相互作用がどのように食欲を調節するのかについては、未だ多くの謎が残されています。この度、研究者チームは、視床下部に存在する新たな神経細胞集団を発見しました。この細胞群は食物摂取を調節し、肥満治療の新たな標的となる可能性があると考えられています。本研究成果は、2024年12月5日付の『Nature』誌に掲載され、「Leptin-Activated Hypothalamic BNC2 Neurons Acutely Suppress Food Intake(レプチン活性化視床下部BNC2ニューロンが急性の食物摂取抑制を誘導する)」というタイトルで公開されました。
この研究は、ロックフェラー大学(米国)、メリーランド大学医学部ゲノム科学研究所(IGS)、ニューヨーク大学、スタンフォード大学の共同研究チームによって行われました。
レプチン応答性ニューロンの発見
視床下部は、食欲調節・ホルモン制御・ストレス応答・体温調節などの生理機能を司る脳の重要な領域です。今回発見された新たな神経細胞群は、ホルモン「レプチン」に応答する特徴を持っています。
レプチンは脂肪細胞から脳へ送られるシグナルで、食欲を抑制する役割を担います。これまで、視床下部の特定のニューロン群がレプチンに応答することは知られていましたが、本研究では、これまで知られていなかった「BNC2ニューロン」が新たなレプチン応答性細胞であることが明らかになりました。
「私たちは以前の研究で、視床下部の発生過程をシングルセル技術でマッピングし、遺伝子の独自の調節プログラムが特殊な神経細胞集団を生み出すことを示しました。その知見を踏まえると、今回の研究で新しい神経細胞が発見されたのは必然的なことでした。」と、IGSのブライアン・ハーブ博士は述べています。
CRISPR-Cas9を用いた肥満の実験モデル
研究チームは、マウスを用いた複数の実験を通じて、BNC2ニューロンが食欲抑制に関与することを明らかにしました。
レプチン受容体(LEPR)を持つBNC2ニューロンを特定
BNC2ニューロンは、食欲抑制や栄養状態に応じた感覚処理を担うことが判明
CRISPR-Cas9を用いた遺伝子ノックアウト実験
BNC2ニューロンのレプチン受容体(LEPR)をノックアウトしたマウスは、食事量が増加し、通常のマウスより体重が増加
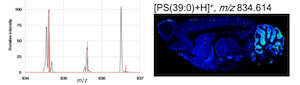
蛍光マーカーによるBNC2ニューロンの可視化
絶食後にマウスに餌を与えた際、BNC2ニューロンが活性化
これまで知られていた視床下部のニューロン群は反応しなかった
「この発見は、食欲と肥満に対する神経調節の理解を大きく前進させるものです」とハーブ博士は述べています。「将来的には、BNC2ニューロンを活性化することで、体重減少や食欲抑制を促進する治療法の開発につながる可能性があります」。
肥満治療の新たな可能性
肥満は世界的な公衆衛生上の課題であり、効果的な治療法の開発が急務です。現在、一部の薬剤が肥満治療に成功を収めていますが、根本的な食欲制御メカニズムの解明はまだ途上です。
本研究で発見されたBNC2ニューロンを標的とする治療法の可能性として、以下が考えられます。
BNC2ニューロンの活性化を促進する薬剤の開発(食欲抑制効果)
遺伝子治療によるBNC2ニューロンの機能回復(レプチン抵抗性の克服)
脳へのレプチンシグナル伝達を強化する新規治療戦略
今後の研究が進めば、これらのアプローチが肥満治療の選択肢を広げる可能性があります。
画像:視床下部は赤色で表示