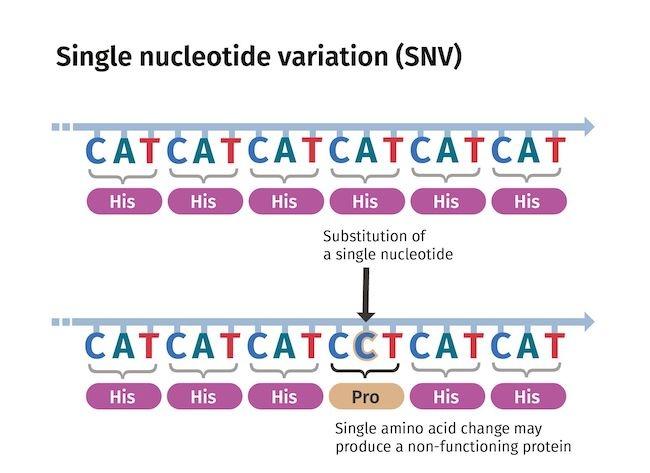
腫瘍の攻撃性やがん患者の特定の治療への反応に、わずか1文字の遺伝子コードの変化が重大な影響を与える可能性があることが、ワイル・コーネル医科大学の研究者らによって明らかにされました。彼らが新たに開発した非常に精密な遺伝子編集ツールにより、この特定の遺伝子変異の影響を前臨床モデルで詳細に研究することが可能となりました。
この画期的なツールの詳細は、2023年8月10日にNature Biotechnology誌に掲載された論文「Generation of Precision Preclinical Cancer Models Using Regulated in Vivo Base Editing(制御されたin vivo塩基編集を用いた高精度前臨床がんモデルの作製)」に記載されています。この研究の筆頭著者であるワイル・コーネル医学部の生化学准教授、ルーカス・ダウ(Lukas Dow)博士は、遺伝子工学的手法を用いて、マウスの遺伝子コードのわずか1文字、すなわち「文字」を変更できる酵素を備えたマウスを創出しました。この酵素は、ドキシサイクリンという抗生物質を投与することでオン・オフ切り替えることができ、時間の経過と共に不意の遺伝子変異の発生リスクを軽減できます。また、研究者たちはマウスから得られた腸、肺、膵臓組織のミニチュアであるオルガノイドを培養することも可能であり、これによって遺伝子変異の影響を分子生物学的および生化学的に更に詳細に調査できます。
ダウ博士は、「この技術を用いて、がん治療における患者の遺伝子変異が治療反応に及ぼす影響を理解することに非常に期待しています」と述べました。ダウ博士はワイル・コーネル医学部のサンドラ&エドワード・マイヤーがんセンターの一員でもあります。
また、ダウ博士は1塩基の遺伝子変化が機能的な影響を持つ可能性を指摘しましたが、現在利用可能な遺伝子編集ツールの多くは遺伝子全体など、より大規模な対象を対象としています。特定の遺伝子変異を導入するためにウイルスを使用する方法もありますが、これは脳や肝臓など特定の組織に限定される技術であるとダウ博士は説明しました。
「遺伝子をノックアウトしたり、遺伝子を過剰発現させたりするための優れたツールは長らく存在してきましたが、患者の腫瘍に見られるような1塩基の急激な変異を引き起こす効果的な手法は存在しませんでした」と、博士は述べました。
このマウスモデルにより、研究者たちは腫瘍に対する変化の影響を探究し、特定の変異を持つ患者に対して最適な治療法を選択する手助けができる可能性が開かれました。さらに、マウス由来のオルガノイドを用いた詳細な実験は、ウイルスベースのアプローチではアクセスが難しかった組織での研究を可能にしています。
ダウ博士は述べました。「この1つのマウスモデルを通じて、2つの重要なことが成し遂げられます。具体的には、特定の遺伝子変異ががんの発生、進行、そして治療反応に及ぼす影響をマウスモデルを用いて評価し、それに関連した分子的および生化学的変化をオルガノイドを通じて詳細に調査することです。」
共同筆頭著者であるアリナ・カッティ博士(元大学院生)とアドリアン・ベガ=ペレス博士(博士研究員)を含むダウ博士と彼の研究チームは、現在、この新技術を用いて、肺がん、結腸がん、膵がんにおける1塩基変異の影響を特定しようとしています。彼らの遺伝子操作マウスモデルは、他の研究者たちにも提供され、個別化がん治療の進展を加速することが期待されています。
ダウ博士は語ります。「私たちはこの技術を他の研究者にも提供し、彼らが興味を持つ変異を研究できるようにしています。腫瘍の発生原因や患者の経過が異なる背後にある遺伝的要因を理解することは、新薬の開発や特定の患者に最適な薬剤の選択に貢献できるでしょう。」