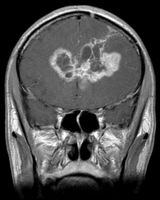
クリーブランド・クリニックの研究者達は、悪性脳腫瘍である悪性グリオーマの腫瘍成長に癌幹細胞が関与するパスウェイを発見した。7月8日にCell誌に発表された記事によると、現在使用されている治療薬は既にこのパスウェイに作用し腫瘍の成長を遅らせ腫瘍をブロックする効果がある事が動物実験により明らかである。致命的なケースが多い脳腫瘍に対し、新しい治療法の提供が可能となってきた。
アメリカで悪性と診断される主たる脳腫瘍は年3,500例以上になり、その半分以上が悪性グリオーマである。悲しい事に、この患者達の見通しは暗い。最も悪性度の高い悪性グリオーマ(グレード?グリオーマ、または多形性神経膠芽細胞腫)の場合、最適と考えられる治療をもってしても、平均生存期間は9−15ヶ月である。その治療というのは、手術後放射線照射と化学療法テモゾロミドを処方し、さらに追加でテモゾロミドを処方する方法を指す。
患者間で腫瘍に違いがあるのは知られていたが、患者中の癌細胞の違いの重要性が理解されはじめたのはごく最近だ。動物モデルでは、グリオーマ内で腫瘍の成長を促進する細胞群−いわゆる癌幹細胞−が確認された。これらの癌幹細胞は放射線と化学療法に耐性があることが多いため、新しい治療法を開発する際に重要な標的とされている。
最近発表された報告書で、クリーブランドクリニック・ラーナー研究所/幹細胞生物学・再生医学部長ジャーミィ・リッチ博士とアニタ・ヘルメランド博士率いる研究チームは、癌幹細胞が腫瘍増殖を促進する際にたどる分子パスウエイを新しく定義した。癌幹細胞では一酸化窒素が過剰に生産されるがその役割ははっきりと解明されておらず、治療に対する耐性、アポトーシスの回避、そして増殖の促進に関与していると考えられている。一酸化窒素は癌幹細胞の一酸化窒素合成酵素?型(NOS2)の増加により生産される。この酵素の生成量や活性の低下により癌幹細胞の成長が遅れる事が分っている。NOS2酵素の抑制薬をグリオーマのあるマウスに投与したところ、腫瘍の成長が減退した。加えて、NIHが提供するデータベースのグリオーマ検体データを元に、NOS2酵素の増加とグリオーマ患者の生存率低下が関連している事が解明された。よって、このパスウエイを標的とすることがグリオーマ治療に有効であると考えられる。
現在の癌治療は様々な副作用を伴う。それは薬剤の癌細胞への感受性を高める事が、正常な細胞へも毒性を高めるからである。そのため、癌の新たな治療法では起こりうる副作用を考慮することが重要となる。今回の研究ではNOS2酵素生成量と、癌幹細胞や正常な神経幹細胞への阻害効果との関連が比較された。正常な神経幹細胞はグリオーマを形成する癌幹細胞と類似する性質を多少もっているが、腫瘍を形成することはない。酵素によって増殖するのは癌幹細胞だけである。NOS2抑制剤をグリオーマ以外の患者に使用する治験における毒性評価の結果は極めて良好であった。報告者等はこれらの薬が副作用無しで現在の治療法に相乗効果をもたらす事が可能であり、NOS2抑制剤が現在致命的な病気の打破につながると示唆している。
[BioQuick News: Discovery May Lead to New Treatment for Malignant Glioma"> [Press release"> [Cell abstract">