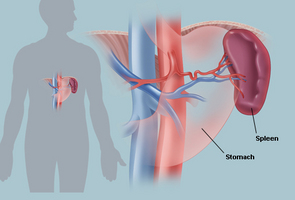
ニューヨーク市にある、ワイルコーネル医科大とロックフェラー大学の研究チームが、脾臓を欠いて生まれてくる無脾症に関連する遺伝子を、初めて同定した。無脾症は感染に対する抵抗が極めて弱いため、この疾患を持った子供達は感染症による死の危険に晒されているのだ。遺伝子Nkx2.5は、マウスにおいては、発生初期の段階で脾臓の創生関与している事が実証された。
この研究はDevelopmental Cell誌の2012年5月3日号オンライン版に発表されたが、簡単な血液検査でNkx2.5の変異を調べることにより、生まれてくる赤ん坊が無脾症である可能性を予測できるというのだ。確定診断はスキャン画像によって行なわれる。「近年では適切な抗生物質の使用により、無脾症の子供達が死に至る事はありません。この診断は予め不慮の死を防ごうとするものなのです。」と主席研究者であり、ワイルコーネル医科大の細胞・発生生物学准教である、リシア・セレリ博士は語る。感染を防御する機構の一部は脾臓が担っているので、無脾症の子供には一生を通して抗生物質の投与計画を建てねばならない。しかし残念な事に現実にはほとんどの場合、致命的な感染症に罹患して肺炎や髄膜炎を起こし、あっと言う間に亡くなった後の剖検で、この先天性無脾症候群である事が判明するのである。
「そういう訳ですから、この症候群は極めて稀だとは言っていられないのです。それに、感染症で亡くなった子供が全ケース剖検されるわけではありません。」とセレリ博士は話す。先天性無脾症候群の患者は、脾臓を欠損するという一つの異常だけを有するのが普通だが、時には心臓や血管に異常を有する場合もある。そのような症例は散発的に見受けられ、遺伝性ではないと考えられる。この疾病の1形態として孤立性先天性脾欠損症(ICA)が知られており、これは脾臓の欠損以外に発生学的な異常は無いのが特徴である。その原因は遺伝性と考えられてはいるが、候補遺伝子はみつかっていない。この研究プロジェクトは、セレリ博士研究室とセントジャイルス研究所感染症人類遺伝学科の教授でロックフェラー大学のジーン・ローレント・カサノバ博士との、共同研究である。
カサノバ博士は、大抵の場合が最初の重篤な感染を1歳時に蒙った、20人のICA患者である子供達を類型化する研究を以前に行なっているが、そのうち9人は侵襲性肺炎によって亡くなっている。セレリ博士はマウスをモデルとして、先天性無脾症候群の研究を長きに渡って続けており、Pbxとして知られる転写因子がマウスモデルにおいて、脾臓の発達を調節する第一の物質であることを発見している。セレリ研究室で最近PhDを取ったマシュー・コス博士は、脾臓にPbxを欠損したマウスの作製に務め、無脾症マウスの作製に成功している。同博士は、Pbxによって調節され、マウス胚にて形成されつつある脾臓に存在しPbxの下流に位置しているNkx2.5を標的とするような、調節モジュールを同定した。同博士はPbxが、Nkx2.5の発現を直接調節しながら脾臓の成長を制御し、それに続いて、
初期の脾臓において細胞増殖を制御していることも発見した。
そしてカサノバ研究室の大学院生であるアレキサンドル・ボルゼ氏が、ICA患者から得たサンプルに全エキソーム解析法を適用して、複数の患者の全コード領域ゲノム解析を行なっているが、この方法はカサノバ研究室ではルーチンとなっている。同氏は、無脾症患者の家族ではNkx2.5に変異があることを発見したが、家族のうち誰かが重篤な感染症で亡くなっている。つまり、マウスモデルにおいて確認されていたNkx2.5の重要性が、ヒトの先天性無脾症候群においても実証されたのである。「この研究によって、マウスモデルとヒト遺伝子研究と相互活用する強みが浮き彫りにされました。マウスモデルにおいて明らかにされた遺伝子パスウエイが、ヒト疾患の病因の解明に役立ち、出生前診断の道を開いたのです。」とセレリ博士は語る。
この疾患の他の形態である患者やその家族については、総合的な別の研究が必要であると、同博士は話す。「他の無脾症の患者のケースでは、他の変異がNkx2.5と一緒に或いは独立して起こっていると考えられます。」と同博士は説明する。これらヒト患者の研究はロックフェラー大学で行なわれ、ワイルコーネル医科大ではマウスモデルの追加研究が進行中である。
■原著へのリンクは英語版をご覧ください: Researchers Discover First Gene Linked to Missing Spleen in Newborns