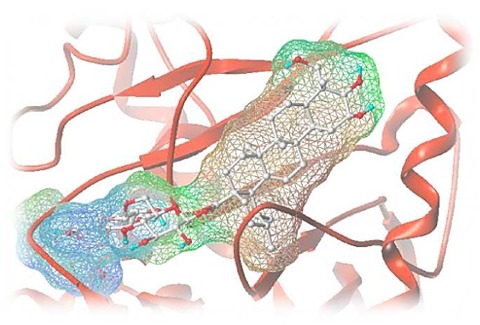
多くの人々を悩ませる関節の痛みに、希望の光が見えてきました。注射一本で、痛みの原因に直接アプローチし、長期間にわたって軟骨を守る――。そんな夢のような治療法が、現実のものとなるかもしれません。ヴァンダービルト大学の研究チームが開発したこの画期的な技術は、私たちの体内に存在するタンパク質「アルブミン」を運び屋として利用する、非常に賢い仕組みです。この新しいアプローチが、つらい関節症の治療をどのように変える可能性があるのか、詳しく見ていきましょう。
賢いsiRNA-脂質複合体が変形性関節症および関節リウマチモデルで長期的な遺伝子サイレンシングと軟骨保護を達成
ヴァンダービルト大学のクレイグ・L・デュバル博士(Craig L. Duvall, PhD)が主導し、フアン・M・コラーゾ医学博士(Juan M. Colazo, MD, PhD)が筆頭著者として発表した画期的な研究が、関節炎治療に革新的なアプローチをもたらします。2025年5月16日に『Nature Biomedical Engineering』誌でオープンアクセス論文として公開されたこの研究は、「siRNA Conjugate with High Albumin Affinity and Degradation Resistance for Delivery and Treatment of Arthritis in Mice and Guinea Pigs(高いアルブミン親和性と分解耐性を備えたsiRNA複合体によるマウスおよびモルモットの関節炎への送達と治療)」と題されています。本研究では、化学的に安定化させ、アルブミンに結合する性質を持たせた低分子干渉RNA複合体を開発し、炎症を起こした関節に直接遺伝子サイレンシング治療を届けることに成功しました。軟骨破壊の中心的な酵素であるマトリックスメタロプロテアーゼ13を標的にすることで、この治療法は変形性関節症と関節リウマチの両モデルにおいて、長期的な保護と症状の緩和を実現します。
関節炎治療における未だ満たされないニーズ
関節炎は、変形性関節症であれ、自己免疫疾患である関節リウマチであれ、世界で最も身体機能を損なう慢性疾患の一つであり続けています。OAの治療は多くの場合、症状を和らげる対症療法であり、非ステロイド性抗炎症薬やコルチコステロイドに依存していますが、これらは長期的に見ると関節の損傷を悪化させる可能性があります。疾患修飾性抗リウマチ薬や生物学的製剤のようなRA治療薬は、免疫活動を抑制しますが、深刻な全身性のリスクを伴い、関節の構造的な変性を防ぐことはできません。
コラーゲンを分解する酵素であるMMP13は、OAとRAの両方で重要な役割を果たしています。合理的な治療標的であるにもかかわらず、薬理学的にMMP13を阻害しようとする試みは、標的外への影響や毒性によって妨げられてきました。関節組織内で安全かつ選択的にMMP13をサイレンシングできる解決策は、関節炎治療の新時代を切り開く可能性があります。
イノベーション:アルブミンに“便乗”するsiRNA
研究チームは、体循環を生き延び、遺伝子のペイロードを病変のある関節に送り届けるための安定性と構造を持つ、化学的に修飾されたsiRNA構築物「siMMP13<(EG18L)₂」を設計しました。その設計には以下の特徴が含まれます。
・ヌクレアーゼ耐性のための、2'-フルオロリボース糖と2'-O-メチルリボース糖を交互に配置した「ジッパー」構造
安定性を高めるためのホスホロチオエート結合
・血清アルブミンへの高い親和性を持つ結合を可能にするための、EG18スペーサーを介して取り付けられた2本のC18脂質尾部
投与されると、このsiRNA構築物は循環するアルブミンに結合し、ELVIS効果(ELVIS: Extravasation through Leaky Vasculature and Inflammatory Sequestration、血管漏出と炎症部位への集積)に導かれて炎症を起こした関節へと追従します。これにより、siRNAは肝臓を迂回し、関節炎組織に直接蓄積することができます。
マウスとモルモットにおける正確な関節ターゲティング
この治療法は、マウスとモルモットの両方の関節炎モデルで検証されました。外傷後OAおよび自己免疫性RAを持つマウスでは、siMMP13<(EG18L)₂を1回静脈内投与したところ、健康な関節と比較して炎症関節で4倍以上の蓄積が達成されました。関節に存在する線維芽細胞、マクロファージ、内皮細胞の90%以上がsiRNAを取り込み、分子は局所的に30日以上持続しました。MMP13の発現は60%以上減少し、肝臓や腎臓などの標的外組織では有意な取り込みやサイレンシングは見られませんでした。
加齢に伴いヒトと同様の様式で自然にOAを発症するモルモットでは、siRNA複合体の関節内注射によっても、強力なMMP13のノックダウン、関節軟骨の維持、およびマトリックス分解マーカーの減少が認められました。著者らはこのモデルで正確な定量的数値を報告していませんが、組織学的および分子的所見は一貫しており、治療効果を強く裏付けるものでした。
疾患修飾効果と構造の維持
両方の動物種にわたり、siMMP13<(EG18L)₂は関節構造の強力な保護をもたらしました。この治療を受けたマウスとモルモットは、軟骨びらんの減少、組織学的スコアの改善、およびC2CフラグメントやmAbCII結合といった軟骨破壊産物のレベル低下を示しました。この治療法は、Zilretta(コルチコステロイド)や、低分子MMP13阻害剤であるCL-82198およびMarimastatの性能を大幅に上回りました。
これらの結果は、圧力感受性や関節の腫れによって評価された関節痛および炎症の軽減を伴いました。
炎症をその源から断つ
MMP13をサイレンシングすることは、構造的な損傷を食い止めるだけでなく、疾患の進行を促進する慢性的な炎症をも断ち切りました。遺伝子発現解析により、NF-κB、p38 MAPK、TLR、そしてTNF、IL-1β、COX-2のようなサイトカインを含む炎症シグナル伝達の広範な抑制が明らかになりました。これらの所見は、MMP13が単なる組織分解酵素ではなく、関節炎の関節における免疫活性化の重要な増幅因子であることを示しています。
自己免疫性関節炎における全身性の有効性
関節リウマチのK/BxNマウスモデルにおいて、siMMP13<(EG18L)₂は強力な全身性の有効性を示しました。この治療法は前足、後足、膝を含む複数の関節に蓄積し、臨床的な関節炎スコア、足首の腫れ、および圧痛を減少させました。組織学的データはパンヌス形成と炎症性浸潤の減少を示し、マイクロCTスキャンは骨構造の維持と骨棘形成の抑制を確認しました。これらの治療効果は、メチルプレドニゾロンとCL-82198の両方を上回るものでした。
主な利点
このsiRNAプラットフォームは、いくつかの魅力的な利点を提供します。
・炎症を起こした関節における正確な遺伝子サイレンシング
・天然のアルブミンをガイドとして利用した全身送達
・1回の注射による長期的な保持
・ナノ粒子やウイルスベクターを回避する、キャリアフリーの化学合成
最小限の標的外毒性と免疫を温存する作用
このプラットフォームのモジュール設計は、さまざまな疾患状況で他の遺伝子を標的とするために迅速に再プログラムすることも可能です。
限界と課題
強力な結果にもかかわらず、臨床応用にはヒトにおける詳細な毒物学および薬物動態の研究が必要です。慢性疾患の管理により適した皮下投与は、同等の有効性を得るために最適化されなければなりません。さらに、大規模合成、GMP製造、および長期安全性プロファイリングが、規制上の進展に不可欠です。
将来の可能性
アルブミンに“便乗”する戦略は、関節炎を越えて広く応用可能です。線維性疾患、炎症性微小環境を持つがん、あるいは疾患部位にアルブミンが蓄積するあらゆる状態に拡張できる可能性があります。このアプローチはまた、標的化され、適応性があり、最小侵襲的であるという、個別化RNA治療の広がりつつあるビジョンとも一致しています。
結論:RNA医療の新たなフロンティア
本研究は、関節炎のような複雑な非肝臓疾患を治療するためにRNA治療をどのように展開できるかについて、臨床的に意義のある飛躍をもたらしました。siRNAを安定化させ、その送達を内因性アルブミンと連携させ、炎症性関節を高い特異性で標的とすることにより、研究者らは免疫抑制、侵襲的ベクター、またはキャリア毒性なしに長期的な遺伝子サイレンシングを達成しました。
誘発性および自然発生性の両方の関節炎モデルにおけるsiMMP13<(EG18L)₂の成功は、このプラットフォームが単なる送達のトリックではなく、MMP13や関節炎だけにとどまらない可能性を秘めた、生物学的に誘導される治療戦略であることを示しています。
RNA医療が拡大を続ける中で、このアプローチは、線維性疾患からがんまで、複数の病態における疾患標的型でキャリアフリーの遺伝子サイレンシングのテンプレートとして機能するかもしれません。より賢く、より安全で、より長持ちする次世代RNA治療薬を設計するための扉が今、開かれました。それは、複雑な疾患のまさに中心に分子レベルの精度を届けるものです。